Die AG besteht zurzeit aus insgesamt 7 Mitarbeitern. Der Schwerpunkt liegt in der Durchführung präklinischer Studien zu implantatassoziierten, vorrangig orthopädischen Fragestellungen. Die Auswertungsmethoden umfassen klinische Parameter, Bildgebung (Röntgen, MRT, CT/µCT), Biomechanik (in enger Zusammenarbeit mit dem Labor für Biomechanik und Biomaterialien) bis hin zu spezialisierten histologischen Techniken (Hartschnitte, Trenn-Dünnschliffe, Immunhistochemie).
Orthopädische Implantate
Orthopädische Implantate werden täglich in der klinischen Routine verwendet, z.B. bei der Versorgung von Knochenbrüchen, Fehlstellungen oder als Gelenkersatz. Dennoch können bei der Nutzung von Implantaten verschiedenste Schwierigkeiten auftreten, wie z.B. Fremdkörperreaktionen des Körpers auf das Material, Knochenabbauprozesse aufgrund von Lastabschirmung oder Implantat-assoziierte Infektionen. Diese oder andere Komplikationen machen eine Implantatentfernung häufig unumgänglich, was mit einer hohen Patientenbelastung verbunden ist. Ein anderes Anwendungsfeld von Implantaten ist beim Auftreten von Sehnen- und Bandabrissen. Häufig kommt es hierbei aufgrund der Schäden oder von degenerativen Prozessen im Falle von chronischen Defekten zu Verlust des ursprünglichen Materials, was eine Refixation insbesondere ohne überbrückende Implantate schwierig bis unmöglich macht.
Forschungsschwerpunkte: abbaubare Implantate für Sehnen und Knochenrekonstruktionen und Implantat-assoziierte Infektionen
Es gibt drei große Schwerpunkte der Forschungsgruppe „Biodegradable und bioaktive orthopädische Implantate“.
Primär wird an der Entwicklung abbaubarer („biodegradabler“) Implantatmaterialien geforscht, die grundsätzlich eine Implantatentfernung nach einer Ausheilung unnötig machen. Dabei steht zum einen die Entwicklung von Implantaten für den Sehnenersatz im Fokus, mit den besonderen Anforderungen, die an Implantate für den Bereich der Enthese gestellt werden. Zum anderen werden degradable metallbasierte Implantate für die Verwendung im knöchernen Bereich entwickelt, wobei hier die fürs belastete Gewebe notwendigen Festigkeiten und ein sehr langsamer Abbau im Vordergrund stehen.
Des Weiteren werden neue Konzepte zur besseren Einheilung von Geweben und Materialien erschlossen sowie an der Vermeidung von Implantatinfektionen durch Prüfung modifizierter („bioaktiver“) Oberflächen und der Evaluation neuer Therapiestrategien gearbeitet.
Bei allen Forschungsschwerpunkten werden zentrale Fragen der mechanischen Stabilität und der Verträglichkeit untersucht. Ziel der Forschungsarbeiten sind optimierte orthopädische Implantatmaterialien und damit eine verbesserte Patientensicherheit und -Lebensqualität.
Im Rahmen einer Vielzahl von Projekten, die von verschiedenen Drittmittelgebern gefördert wurden, u.a. von der Deutschen Forschungsgemeinschaft (DFG) im Rahmen des Sonderforschungsbereichs 599 „Zukunftsfähige bioresorbierbare und permanente Implantate aus metallischen und keramischen Werkstoffen“, konnte ein breites Methodenspektrum entwickelt und etabliert werden. So können Implantate präklinisch sowohl auf ihre Verträglichkeit als auch auf ihre Funktionalität geprüft werden.
Dabei kommen zum einen in vitro Verfahren zur Untersuchung des Degradationsverhaltens neuer abbaubarer Materialien und Zellkultur-Testsysteme zur Evaluierung der Zytotoxizität zum Einsatz. Zum anderen erfolgt die Prüfung der notwendigen Funktionsbeständigkeit von Implantaten mittels biomechanischer Methoden wie Zug- und Biegeversuchen sowie zyklischer Testverfahren. Weiterhin sind eine Vielzahl spezifischer Tiermodelle für die präklinische Prüfung in vivo etabliert. Zur Auswertung werden bildgebende Verfahren ebenso verwendet wie diverse histologische Methoden. Als Nicht-invasive Nachweismethoden können neben einem Fluoreszenz Imaging System zur in vivo Untersuchung von Entzündungsreaktionen oder pH-Wertverschiebungen im Kleintier in Kooperation mit dem Institut für Versuchstierkunde der MHH ein in vivo Mikro-CT-Scanner und ein hochauflösender Magnet-Resonanz-Tomograph genutzt werden. Damit können beispielsweise fortschreitender Implantatabbau oder knöcherne Integration zu unterschiedlichen Zeitpunkten quantitativ erfasst werden.
Neben gängigen histologischen Untersuchungstechniken einschließlich der Fluoreszenzmikroskopie wird die Konfokale Laser-Scanning Mikroskopie in Zusammenarbeit mit der Zentralen Forschungseinrichtung für Lasermikroskopie der MHH oder der Klinik für Zahnärztliche Prothetik und Biomedizinische Werkstoffkunde hier im NIFE für die Untersuchung von Implantatoberflächen genutzt.

In der Entwicklung von Implantaten für den Sehnenersatz wird innerhalb einer von der DFG geförderten Forschergruppe in enger, interdisziplinärer Zusammenarbeit mit Instituten der Leibniz Universität sowie des Helmholtz Instituts in Braunschweig geforscht (FOR 2180 – Sehnen- und Knochenverbindungen). Im Fokus der Arbeitsgruppe stehen dabei die Überprüfung der in vitro gewonnen Ergebnisse in einem klinisch sehr anwendungsnahen Tiermodell, das die Beurteilung unter Berücksichtigung der Wirkung der Implantate auf den Gesamtorganismus erlaubt.

Abbaubare Implantatmaterialien stellen nicht nur einen Vorteil beim Einsatz im klassischen Bereich Frakturheilung dar, sondern können durch ihre Wirkung, den Knochenzuwachs anzuregen, auch in andere Gebiete übertragen werden. So wird aktuell der Einfluss von magnesiumbasierten Beads auf die subchondrale Knochenstruktur im Knie untersucht, um so die Progessionsgeschwindigkeit von degenerativen Knorpelveränderungen im Zuge von Osteoarthrose positiv zu beeinflussen.
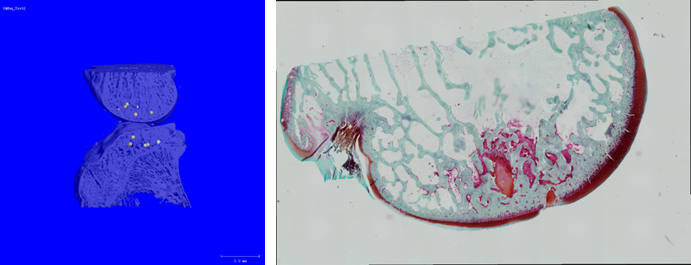
Im Bereich der Implantat-assoziierten Infektionen wird derzeit ein therapeutischer Ansatz verfolgt. Hierbei steht ein Verfahren im Forschungsfokus, bei welchem an Nanopartikel gebundene Chemotherapeuthika gezielt am gewünschten Wirkort, der Implantatoberfläche, akkumuliert werden können. So sollen einerseits die Gefahr von Nebenwirkungen durch systemische Gaben zu verringert und andererseits die therapeutisch notwendige Konzentration vor Ort sicher erreicht werden. Für die Akkumulation der Nanopartikel wird ein elektromagnetisches Feld im Implantationsbereich genutzt. Ziel dieses Verfahrens ist es, bei einer später auftretenden Infektion zu einem beliebigen Zeitpunkt nach der Implantation eine Therapieoption zu schaffen, die eine Implantatentfernung vermeidet.

Aktuelle Projekte:



Aktuelle Publikationen:
Angrisani N, Willbold E, Kampmann A, Derksen A, Reifenrath J.
Histology of tendon and enthesis - suitable techniques for specific research questions.
Eur Cell Mater. 2022 May 24;43:228-251. doi: 10.22203/eCM.v043a16.
Angrisani N, Willumeit-Römer R, Windhagen H, Mavila Chathoth B, Scheper V, Wiese B, Helmholz H, Reifenrath J.
Small-sized magnesium cylinders influence subchondral bone quality in osteoarthritic rabbits - an in vivo pilot study.
Eur Cell Mater. 2021 Sep 28;42:179-195. doi: 10.22203/eCM.v042a14.
Floerkemeier T, Budde S, Willbold E, Schwarze M, Niehof M, Lichtinghagen R, Windhagen H, Weizbauer A, Reifenrath J.
Do biomarkers allow a differentiation between osteonecrosis of the femoral head and osteoarthritis of the hip? - a biochemical, histological and gene expression analysis.
Osteoarthritis Cartilage. 2021 Nov;29(11):1614-1623. doi: 10.1016/j.joca.2021.08.006. Epub 2021 Aug 26.
J, Janßen HC, Warwas DP, Kietzmann M, Behrens P, Willbold E, Fedchenko M, Angrisani N. Implant-based direction of magnetic nanoporous silica nanoparticles - influence of macrophage depletion and infection. Nanomedicine. 2020 Aug 26;30:102289. doi: 10.1016/j.nano.2020.102289.
Willbold E, Wellmann M, Welke B, Angrisani N, Gniesmer S, Kampmann A, Hoffmann A, de Cassan D, Menzel H, Hoheisel AL, Glasmacher B, Reifenrath J. Possibilities and limitations of electrospun chitosan-coated polycaprolactone grafts for rotator cuff tear repair. J Tissue Eng Regen Med. 2020 Jan;14(1):186-197. doi: 10.1002/term.2985.
Schröder ML, Angrisani N, Fadeeva E, Hegermann J, Reifenrath J. Laser-structured spike surface shows great bone integrative properties despite infection in vivo. Mater Sci Eng C Mater Biol Appl. 2020 Apr;109:110573. doi: 10.1016/j.msec.2019.110573.
Reifenrath J, Wellmann M, Kempfert M, Angrisani N, Welke B, Gniesmer S, Kampmann A, Menzel H, Willbold E. TGF-β3 Loaded Electrospun Polycaprolacton Fibre Scaffolds for Rotator Cuff Tear Repair: An in Vivo Study in Rats. Int J Mol Sci. 2020 Feb 5;21(3):1046. doi: 10.3390/ijms21031046.
Janßen HC, Angrisani N, Kalies S, Hansmann F, Kietzmann M, Warwas DP, Behrens P, Reifenrath J. Biodistribution, biocompatibility and targeted accumulation of magnetic nanoporous silica nanoparticles as drug carrier in orthopedics. J Nanobiotechnology. 2020 Jan 15;18(1):14. doi: 10.1186/s12951-020-0578-8.

PD Dr. med. vet. Janin Reifenrath
+49 511 532 8961
Reifenrath.janin(at)mh-hannover.de
NIFE
Stadtfelddamm 34
30625 Hannover
Aktuelle Projekte: